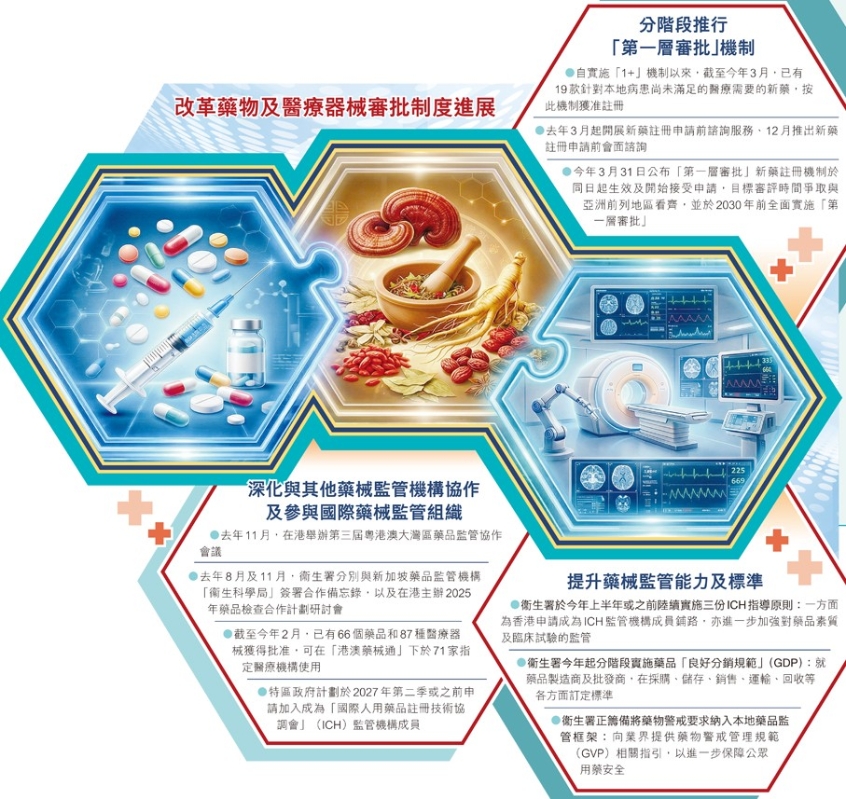
香港藥械審批重要改革:中西藥監管權統一至衛生署署長香港新聞網4月9日電 香港藥物及醫療器械監管領域進行重要改革。香港特區政府醫務衞生局向立法會衞生事務委員會提交文件,就成立香港藥物及醫療器械監督管理中心提出立法建議,包括確立藥械監管中心的法定地位及定位、轉移藥物監管權力、優化現時藥物監管架構等,其中備受關注是將中、西藥物的監管權力轉移至衞生署署長,以統整中、西藥的監管職能,理順監管架構,並與國際標準銜接。特區政府計劃在今年下半年將《條例草案》提交立法會審議。 據香港文匯報報道,醫務衞生局指出,特區政府計劃在今年下半年提交《條例草案》,聚焦於在衞生署下成立藥械監管中心,負責與藥械監管相關的職能。條例草案同時將修訂現時分別規管西藥(即藥劑製品)和中藥的《藥劑業及毒藥條例》(第138章)及《中醫藥條例》(第549章),將藥物監管權力轉移至衞生署署長,以統整中、西藥的監管職能,理順監管架構,並與國際標準銜接。 文件進一步解釋,《條例草案》會修訂《藥劑業及毒藥條例》及其附屬法例,將現時藥劑業及毒藥管理局及其屬下委員會監管藥劑製品及相關牌照商的權力轉移至衞生署署長。而藥劑業及毒藥管理局及相關委員會會予以保留,就藥劑製品的監管向衞生署署長提供意見。 《條例草案》亦會對《中醫藥條例》及其附屬法例作出相應修訂,將現時中藥組及其屬下小組監管中藥/中成藥及中藥牌照商的權力轉移至衞生署署長,而中藥組及相關小組會予以保留,並會就中藥/中成藥的監管向衞生署署長提供意見。 至於藥劑師及中醫監管方面,藥劑業及毒藥管理局、香港中醫藥管理委員會及其屬下的中醫組將繼續履行相關權力及責任,維持現狀不變。醫務衞生局指,這項修訂符合國際上普遍將專業規管與藥物及相關牌照商規管分開的做法。 文件指,是次修訂會將決策權力統一交由衞生署署長行使,並將藥劑業及毒藥管理局、中藥組及各委員會、小組轉為擔任諮詢角色,就相關監管事宜向署長提供意見,減少架構上的重疊,有助縮短決策鏈條,提升整體監管效率。這亦能大幅提升兩套制度在運作上的一致性,為業界提供更清晰、統一的規管環境,推動中、西藥監管制度在架構及程序上逐步融合。 此外,局方亦藉此機會完善藥物規管的上訴機制,提供向原訟法庭提出上訴以外的申訴渠道。 醫療器械規管方面,文件指《條例草案》並不包括規管醫療器械方面的條文。特區政府正推進相關立法準備工作,因應近年國際間最新規管趨勢,全面檢討擬議規管架構,將於今年內向立法會提交立法建議。
藥械監管中心是香港特區改革藥械審評審批和監管制度的重要里程碑。醫療衞生界立法會議員林哲玄指出,成立該中心的關鍵在於統一標準與操作系統,提升監管能力和審批能力,重點是要擁有藥械第一層審批的能力,才能吸引全世界科研製藥機構落戶香港。關注病人權益的組織則期望,香港藥械監管中心成立後可對醫療器械進行規管,尤其是美容領域的器械,以保障病人安全。 今次《條例草案》提出賦權衞生署署長監管中、西藥以及成立藥械監管中心。香港病人政策連線主席林志釉昨日向媒體表示,若香港藥械監管中心專門負責檢視這些西藥、中藥的安全性,對病人有好處。 林志釉又關注醫療器械的監管,“我們經常看到相關情況,甚至醫務委員會一些投訴都涉及醫療器械,可能是醫療效果的問題,亦可能是這些器械缺乏監管。”他舉例,坊間美容院的激光儀、聲波儀、電療儀等,“如果這些器械有一定醫療效果,那麼這些器械都必須有相應監管,才能保障病人安全,例如機器是否符合相關安全標準?”他期望,藥械監管中心日後能制定更多醫療器械方面的規範要求。 林哲玄向媒體表示,成立香港藥械監管中心的關鍵在於統一標準與操作,監管方式和標準要一致,對質量保證更穩妥。“重點在於先要擁有(藥械)第一層審批的能力,香港才能吸引全世界科研製藥機構落戶香港,從事藥物研發,發展產業鏈、註冊、銷售。” 他強調,香港在科研方面與世界接軌,得到世界普遍認同,期望將來無論是香港獨自研發,還是與內地共同研發的新藥械,在香港第一層審批後可推向世界,發揮背靠祖國、聯通世界的“超級聯繫人”角色,貢獻國家所需。(完) 【編輯:王少喆】
|